□ 식품의약품안전처(처장 김강립)는 한국노바티스㈜가 허가 신청한 세계 최초 키메라 항원 수용체 T세포(CAR-T) 치료제 ‘킴리아주(티사젠렉류셀)’를 「첨단재생바이오법」1)에 따른 제1호 첨단바이오의약품2)으로 허가했습니다.
1) 「첨단재생의료 및 첨단바이오의약품 안전 및 지원에 관한 법률」(약칭: 첨단재생바이오법) : 첨단바이오의약품 특성에 맞는 차별화된 안전관리 및 제품화 지원을 위해 ’20.8.28. 시행
2) 세포치료제·유전자치료제 등 살아있는 세포·조직이나 유전물질 등을 원료로 한 의약품
○ ‘키메라 항원 수용체(chimeric antigen receptor) T세포’는 면역세포(T세포)의 수용체 부위와 암세포 표면의 특징적인 항원 인식 부위를 융합한 유전자를 환자의 T세포에 도입한 것으로, 암세포의 표면 항원을 특이적으로 인지해 공격하는 기능을 갖는 세포입니다.
□ ‘킴리아주’는 환자로부터 채취한 면역세포(T세포) 표면에 암세포의 특정 항원을 인지할 수 있도록 유전정보를 도입한 후 환자의 몸에 주입하는 방식의 항암제입니다.
○ 이 약은 다른 치료제를 선택하는 것이 제한적인 재발성·불응성 혈액암 환자1)에게 한 번의 투여로 명백히 개선된 유익성을 보인 혁신적 면역세포 항암제로, 미국에서는 획기적 의약품(Breakthrough designation), 유럽에서는 우선순위의약품(PRIME)으로 각각 지정된 후 허가2)받았습니다.
1) 재발성·불응성인 ▲25세 이하 B세포 급성 림프구성 백혈병 ▲미만성 거대 B세포 림프종
2) 해외 허가 현황 : [미국] 2017.8. [유럽] 2018.8. [일본] 2019.3. 등
○ 식약처는 「첨단재생바이오법」의 심사기준에 따라 신청 의약품에 대한 품질, 안전성·효과성, 시판 후 안전관리계획 등에 대해 과학적으로 철저하게 심사·평가했으며
- 혈액암 분야 의료현장 전문가 등이 포함된 중앙약사심의위원회에서 해당 제품의 허가 타당성과 제도 부합성에 대한 자문을 거쳤습니다.
○ 특히 이 약은 「첨단재생바이오법」 제30조에 따른 ‘장기추적조사’* 대상 의약품으로, 이상사례 현황에 대해 투여일로부터 15년간 장기추적해야 하며, 최초 판매한 날부터 1년마다 장기추적조사한 내용과 결과 등을 식약처에 보고해야 합니다.
* 장기추적조사 : 줄기세포 또는 동물의 조직·세포를 포함하는 첨단바이오의약품이나 투여 후 일정기간동안 이상사례의 발생 여부를 확인할 필요가 있을 경우 5-30년 이내의 추적 기간 부여
□ 식약처는 “이번 품목 허가가 대체의약품이 없거나 표준치료법이 확립되지 않은 재발성·불응성 혈액암 환자에게 새로운 치료 기회를 제공할 수 있을 것이라 기대한다”며
○ “앞으로도 국민이 안심할 수 있도록 첨단바이오의약품의 세포 채취부터 사용 후 단계까지 안전하게 관리해 나가겠다“라고 밝혔습니다.
<붙임> 제품 허가사항(요약)
<붙임> 제품 허가사항(요약)
❍ 제품명/회사명 : 킴리아주(티사젠렉류셀)/한국노바티스(주)
❍ 제제분류 : 첨단바이오의약품 중 유전자치료제
❍ 효능효과 :
1. 25세 이하의 소아 및 젊은 성인 환자에서의 이식 후 재발 또는 2차 재발 및 이후의 재발 또는 불응성 B세포 급성 림프성 백혈병(ALL)의 치료
2. 두 가지 이상의 전신 치료 후 재발성 또는 불응성 미만성 거대 B세포 림프종(DLBCL) 성인 환자의 치료
❍ 작용기전
- 키메라 항원 수용체(chimeric antigen receptor, CAR)를 코딩하는 외래도입유전자(transgene)를 환자 본인의 T세포에 도입하여 CD19 발현 세포를 구분해 제거하도록 유전적으로 변형된 자가 면역세포 항암제
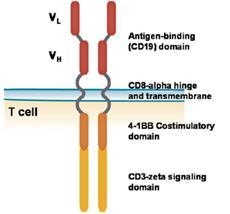
참고 | | CAR-T 세포 |
❍ CAR-T 세포란?
T세포 수용체와 암세포 표면의 특징적인 항원 인식 부위를 융합한 유전자를 환자의 T 세포에 유전자를 도입한 후 암세포의 표면 항원을 특이적으로 인지하여 공격하도록 하는 기능을 부여한 세포
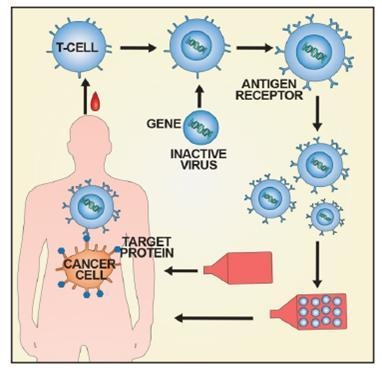
❍ CAR-T 의 제조 및 투여과정
- 1단계 : single chain Fv(scFv) 전이 유전자 포함된 벡터 제조
- 2단계 : T 세포에 벡터 도입
- 3단계 : 키메릭 항원 수용체 유전자 도입된 T 세포 증식 및 투여